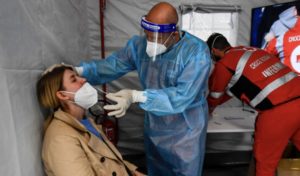
La pillola anti Covid all’esame della Fda per l’uso d’emergenza
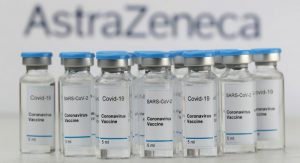
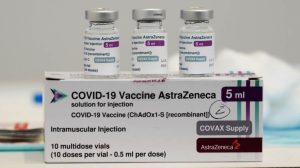
La casa farmaceutica statunitense Merck ha annunciato oggi di aver richiesto all’Agenzia del farmaco e dell’alimentazione (Fda) l’autorizzazione per l’uso d’emergenza della sua pillola sperimentale antivirale molnupiravir, usate per la cura del Covid-19. Se dovesse ricevere l’autorizzazione, il farmaco – prodotto da Merck e Ridgeback Biotherapeutics, sarebbe il primo con somministrazione orale a essere utilizzato per il trattamento della malattia. La pillola verrebbe usata da adulti che sono a rischio di contrarre forme gravi del Covid-19: in base agli studi presentati, infatti, riducono il rischio di ricovero in ospedale o di morte di circa il 50 per cento.
Autorizzazione della pillola chiesta in tempi record
«L’impatto straordinario di questa pandemia ci impone di muoverci con straordinaria urgenza, ed è quello che abbiamo fatto presentando richiesta all’Fda entro dieci giorni dalla ricezione dei dati», ha spiegato in un comunicato il presidente e amministratore delegato di Merck Robert Davis.In vista di un potenziale via libera, Merck spiega di aver cominciato a produrre molnupiravir e di prevedere di arrivare alla produzione di 10 milioni di cicli di trattamento entro fine 2021.
Che cos’è il molnupiravir
Il molnupiravir è un antivirale che è stato sviluppato inizialmente contro altri virus, come quelli influenzali, ma quando è scoppiata la pandemia è stato “dirottato” su Sars-Cov-2 e sperimentato sui primi pazienti con Covid-19. I dati diffusi dall’azienda riguardano 762 pazienti adulti (non vaccinati) con Covid-19 lieve e moderato ma a rischio di malattia grave per obesità, età avanzata, diabete o malattie cardiovascolari, cui è stato dato il farmaco o il placebo. Dopo 29 giorni dalla somministrazione i ricercatori hanno osservato che nel gruppo di volontari che aveva assunto l’antivirale il rischio di ospedalizzazione o morte si era dimezzato rispetto a quello cui era stato dato il placebo: il 7,3% dei pazienti che aveva ricevuto molnupiravir era stato ricoverato in ospedale o era deceduto, contro il 14,1% dei pazienti trattato con il placebo. La sperimentazione, che in origine doveva continuare fino a prevedere il coinvolgimento di 1.500 volontari, è stata interrotta in anticipo per “manifesta superiorità del farmaco” rispetto al placebo, così che potesse essere dato a tutti un farmaco ormai ritenuto efficace: sarebbe stato scorretto proseguire, privando quelli cui veniva destinato il placebo del beneficio derivante dal medicinale.
Criticità della pillola
Il trattamento prevede che il farmaco venga somministrato presto, entro 5 giorni dall’esordio dei sintomi. Il trattamento, poi, non è indicato per tutti i malati: l’utilizzo nei pazienti già ospedalizzati non è considerato promettente. Il molnupiravir non potrà essere utile a chi si aggrava velocemente tanto da richiedere il ricovero in tempi brevi. E non potrà essere utilizzato nelle donne gravide, perché come altri farmaci antivirali, ha un potenziale mutageno delle cellule.
All’esame dell’Ema i monoclonali
«L’Agenzia europea per i medicinali (Ema) ha avviato la valutazione su una domanda di autorizzazione all’immissione in commercio per la combinazione di anticorpi monoclonali Ronapreve (casirivimab/imdevimab). Il richiedente è Roche Registration Gmbh». Lo si apprende da una nota dell’Ema. Il farmaco Ronapreve, si legge, «è destinato al trattamento del Covid-19 negli adulti e negli adolescenti dai 12 anni di età che non richiedono ossigeno supplementare e che sono a maggior rischio di progressione alla forma grave» e, più in generale, «per la prevenzione del Covid-19 negli adulti e negli adolescenti dai 12 anni in su». «L’Ema valuterà i benefici e i rischi di Ronapreve in tempi ridotti e potrebbe emettere un parere entro due mesi», precisa la nota.
© RIPRODUZIONE RISERVATA